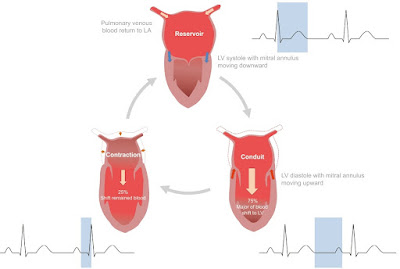
En amiloidosis cardíaca (AC) la infiltración por proteína fibrilar amiloide anómala altera el acortamiento longitudinal base-punta del VI así como las funciones fásicas de la aurícula izquierda (AI).
Inoue
y cols. estudiaron retrospectivamente 341 pacientes con diagnóstico confirmado
de hipertrofia ventricular izquierda patológica (RNM, SPECT, biopsia tisular)
con Fey normal. Sus objetivos fueron evaluar la relación entre la deformación
basal VI y el SR del reservorio de la AI en hipertrofia VI patológica, así como
su capacidad para identificar etiología de AC y su posible valor predictivo
para la hospitalización por insuficiencia cardíaca (IC). (Inoue et al. Cardiovascular
Ultrasound 2025 )
El SR
longitudinal VI (<16%) correlacionó con el SR del reservorio de AI (<18%)
en el grupo con AC (75p, r = 0,58, p < 0,01) y en el grupo sin AC (266p, r =
0,44, p < 0,01). Se comprobó que el SR longitudinal apical junto a la
relación E/e´ septal y al SR de reservorio AI permitieron discriminar grupos
con AC y sin AC (Regresion log. binaria, p < 0,01). El SR longitudinal basal-apical
tuvo mejor capacidad (ABC 0,90) que el SR de reservorio AI (ABC 0,81) para
discriminar entre AC y etiologías sin AC. En el seguimiento (2,7 años) la
incidencia de hospitalización por IC fue mayor en grupo con AC que sin AC (35%
vs. 14%; p <0,001) encontrándose que las variables SR reservorio AI (<18%),
E/e´ e índice de volumen AI estuvieron asociadas a hospitalización por IC en el
grupo sin AC (análisis de regresión de Cox, p <0,05).
Concluyeron
que el SR del reservorio AI se asoció estrechamente con SR longitudinal VI con
valor adicional a este último, especialmente en pacientes con etiología de AC
que además permite discriminar la AC de otras etiologías de HVI.
(Inoue et al. Cardiovascular Ultrasound 2025 )
Limitaciones: Aunque se describió la elevada factibilidad para obtener imágenes del SR de reservorio AI (95%); también deberían comunicarse las dificultades técnicas y/o variabilidad de adquisición de las imágenes: ventana acústica y nivel de experiencia/variabilidad intra/inter-operador. El ecocardiógrafo, el software y el algoritmo para el análisis del strain fue descripto.
Por
ser unicéntrico y retrospectivo el “n” de casos con AC resultó muy bajo para
predicción de evolución a IC, pero eleva la hipótesis para estudios
prospectivos de mayor tamaño. Probable sesgo de selección/ejecución con
aquellos casos que no pudieron ser estudiados para diferenciar subtipos de AC
(TTR vs. AL) y etiología de HVI.